Die Wasserqualitaet
Beurteilung der natürlichen Wässer
Grundwasser
Grundwasser (Brunnen- und Quellwasser) ist im allgemeinen arm an groben Verunreinigungen
(Bodenfiltrierung) und bedarf daher selten einer besonderen Klärung. Dagegen enthält es sehr oft
aggressive Kohlensäure, Eisen und wenig Sauerstoff.
Oberflächenwasser
Oberflächenwasser (Fluss-, See- und Teichwasser) kann durch Abwasser, Laubabfall,
Hochwassereinflüsse verunreinigt werden. Es bedarf daher einer besonderen Klärung. Infolge guter
Belüftung ist die aggressive Kohlensäure gering und der Sauerstoffgehalt
hoch.
Bestimmung der Wasserqualität
Wasserhärte Unter Härte eines Wassers versteht man seinen Gehalt an
gelösten Erdalkali-, besonders an Calcium- und Magnesium-Salzen. Aus
Calcium- und Magnesiumkarbonat (Karbonathärte KH) entstehen beim
Erhitzen des Wassers schwerlösliche Niederschläge (Kesselstein). Die
Erdalkalichloride und Sulfate (Nichtkarbonathärte NKH) sind weniger
schwer löslich. Sie werden erst beim Eindampfen des Wassers ausge-
schieden. Die Gesamthärte ist die Summe von Karbonat- und
Nichtkarbonathärte: GH = KH + NKH
Härte-Begriffe
0-7 °f = sehr weich, 7-14 °f = weich, 4-22 °f mittel hart, 22-31 'f =
hart, über 32 °f = sehr hart
1 °f.H = 0,56 °d.H = 0,2 mval/kg = 0,1 mmol/l = 10,0 ppm =10g
Kalziumkarbonat pro m3 Wasser.
Leitfähigkeit des Wassers
Bei Wasser, in welchem noch Spuren von Salzen gelöst sind, wird die
Menge der gelösten Salze an hand der elektrischen Leitfähigkeit be-
stimmt. Die gemessene (spezifische) Leitfähigkeit wird in
Mikrosiemens/cm ausgedrückt. 1 Mikrosiemens/cm entspricht der
Leitfähigkeit einer Lösung von ca. 0,5 mg NaGI (Natriumchlorid) oder 0,1
mg HGI (Salzsäure) oder 0,2 mg NaOH (Natron-Lauge) pro Liter Wasser.
Definiert wird die Leitfähigkeit als der elektrische Widerstand einer
Flüssigkeit. Die Leitfähigkeit ist der Kehrwert des Widerstandes. Je kleiner der Leitwert, desto reiner
das Wasser.
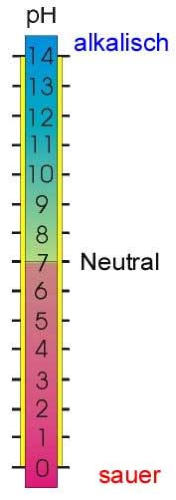
Der pH-Wert
Der pH-Wert ist ein Mass tür die Menge an Wasserstoffionen, die in 1 Liter Wasser effektiv vorhan-
den sind. Je saurer eine Lösung ist, um so kleiner ist der pH-Wert, umgekehrt nimmt mit steigender
Alkalität der pH-Wert zu. Der pH-Wert von neutralem Wasser ist 7.
Die Änderungen um eine ganze pH-Zahl ändert den sauren oder alkalischen Charakter um das
10fache.